Kv1.3 İnhibisyonu, Mikroglial Kalsiyum Sinyalinin Bozulması Yoluyla Nöroinflamasyonu Azaltır
Jul 07, 2023
SOYUT
Son 5 yılda potasyum kanalı KV1.3 inhibitörlerinin iskemik inme, Alzheimer hastalığı, Parkinson hastalığı ve travmatik beyin hasarı kemirgen modellerinde nöroinflamasyonu azalttığı gösterilmiştir. Sistemik düzeyde, bu yararlı etkilere mikroglia aktivasyonundaki bir azalma ve proinflamatuar sitokin ve nitrik oksit üretiminin baskılanması aracılık eder.
Bununla birlikte, KV1.3 blokerlerinin proinflamatuar mikroglia fonksiyonları üzerindeki baskılayıcı etkisine yönelik moleküler mekanizmalar, grubumuz yakın zamanda KV1.3 kanallarının voltaj kapılı bir potasyum kanalından bekleneceği gibi sadece membran potansiyelini düzenlemediğini gösterene kadar bilinmiyordu. , aynı zamanda mikroglia'nın ATP tehlike sinyali tarafından üretilen depolarizasyonlara direnmesini sağlamada ve böylece P2X4 reseptörleri aracılığıyla kalsiyum akışını düzenlemede çok önemli bir rol oynar. Burada KV1.3'ün mikroglial sinyallemedeki rolünü gözden geçiriyoruz ve T hücrelerindeki rollerine benzer şekilde, KV1.3 kanallarının da mikrogliada mağaza tarafından işletilen kalsiyum akışını düzenlediğini gösteriyoruz.
Potasyum kanalı KV1.3, hücre zarı potansiyelinin, hücre göçünün ve bağışıklık hücresi fonksiyonunun düzenlenmesinde önemli bir rol oynayan, bağışıklık hücrelerinde yaygın olarak ifade edilen bir iyon kanalıdır. Son araştırmalar, potasyum kanalı KV1.3'ü inhibe eden bileşiklerin vücudun bağışıklığını artırmaya yardımcı olabileceğini düşündürmektedir.
Bağışıklık sistemini düzenlemek, sağlığı korumanın önemli bir parçasıdır. Bununla birlikte, otoimmün hastalıklar, kanser ve bulaşıcı hastalıklar gibi birçok hastalık, işlevsiz bir bağışıklık sistemi ile sonuçlanır. Bu nedenle, araştırmacılar bağışıklığı artırmanın yollarını arıyorlar. Son araştırmalar, potasyum kanalı KV1.3 inhibitörlerinin umut verici bir seçenek olabileceğini düşündürmektedir.
Bağışıklık hücrelerinde potasyum kanalı KV1.3, zar potansiyelini düzenleyerek hücre fonksiyonunu etkiler. Çalışma, potasyum kanalı KV1.3'ü inhibe ederek, T hücrelerinin göçünü azaltmanın ve sağlıklı hücrelere saldırmalarını önlemenin mümkün olduğunu ve böylece bağışıklık sistemini gereksiz yıkımdan koruduğunu buldu.
Ek olarak, bazı deneyler potasyum kanalı KV1.3'ün engellenmesinin bağışıklık sisteminin diğer yönlerini de destekleyebileceğini bulmuştur. Örneğin araştırmalar, bu kanalın engellenmesiyle bağışıklık hücrelerinin nitelik ve niceliğinin artırılabileceğini ve böylece vücudun patojenlere ve diğer dış tehditlere karşı direncinin artırılabileceğini göstermiştir. Bu nedenle, potasyum kanalı KV1.3'ün inhibisyonu, bağışıklığı güçlendirmenin etkili bir yolu olabilir.
Sonuç olarak, mevcut çalışma, potasyum kanalı KV1.3'ün inhibisyonunun, bağışıklık sisteminin işlevini iyileştirmek ve vücudun genel bağışıklığını artırmak için umut verici bir yaklaşım olabileceğini düşündürmektedir. Ancak bu bulgular umut verici olsa da, bu yaklaşımı kullanmanın güvenliğini ve fizibilitesini belirlemek için daha fazla araştırmaya ihtiyaç vardır. Bu açıdan bağışıklığımızı güçlendirmemiz gerekiyor. Cistanche, bağışıklığı önemli ölçüde artırabilir. Et külü, bağışıklık sistemini uyarabilen polisakkaritler, iki mantar ve Huang Li gibi çeşitli biyolojik olarak aktif bileşenler içerir. çeşitli hücre türleri, bağışıklık aktivitelerini arttırır.

Cistanche'nin sağlığa faydalarına tıklayın
giriiş
Voltaj kapılı potasyum kanalı KV1.3 ilk olarak T hücrelerinde [1] tanımlanmış ve daha sonra multipl skleroz, romatoid artrit ve sedef hastalığı gibi T hücresi aracılı otoimmün hastalıkları tedavi etmek için bir hedef olarak izlenmiştir [2-4]. Daha yakın zamanlarda KV1.3, mikroglia aktivasyonunu modüle ederek sözde "nöroinflamasyonu" azaltmak için çekici bir farmakolojik hedef olarak ortaya çıkmıştır. İskemik inmenin hem fare hem de sıçan modellerinde, KV1.3 blokerlerinin enfarktüs alanını azalttığı ve nörolojik defisitleri iyileştirdiği tarafımızdan ve başkaları tarafından gösterilmiştir [5,6]. Alzheimer hastalığının transgenik fare modellerinde KV1.3 blokajı serebral amiloid yükünü azalttı, hipokampal nöronal plastisiteyi arttırdı ve davranış kusurlarını iyileştirdi [7].
Benzer şekilde, küçük moleküllü KV1.3 bloker PAP-1'nin Parkinson hastalığı olan birçok hayvan modelinde uygulanması, dopaminerjik nöronların dejenerasyonunu önledi ve davranışsal sonuçları iyileştirdi [8]. KV1.3 inhibisyonunun veya genetik delesyonun ayrıca travmatik beyin hasarı [9], postoperatif kognitif gerileme [10] ve radyasyona bağlı beyin hasarı [11] sonrasında beyaz cevher patolojisini iyileştirdiği gösterilmiştir. Tüm bu nörolojik hastalık hayvan modellerinde, patolojiyle ilişkili mikroglia üzerinde artmış KV1.3 ekspresyonu gözlemlendi ve KV1.3 blokerleri ile tedavi, mikroglia aktivasyonunun azalmasına ve hayvanların beyinlerinde enflamatuar sitokin düzeylerinin düşmesine neden oldu.
Hastalıkla ilişkili artmış KV1.3 ekspresyonu insanlara tercüme ediliyor gibi görünmektedir, çünkü güçlü KV 1.3 ekspresyonu postmortem insan beyinlerinde iskemik inmeyi takiben enfarktüslü alanlarda mikroglia üzerinde [5,12], Alzheimer hastalığında amiloid plakları çevreleyen mikroglia üzerinde de bulunmuştur [ 7,13] ve Parkinson hastalığında prefrontal korteksteki mikroglia ve substantia nigra [8]. Birlikte ele alındığında, insan ve hayvan modellerindeki bu cesaret verici bulgular, mikroglial KV1.3 kanallarının beyindeki zararlı inflamatuar yanıtları azaltmak için terapötik bir hedef olduğunu kuvvetle önerir. Ancak KV1.3 engelleyiciler nasıl çalışır? Mikrogliada voltaj kapılı bir potasyum kanalını ve muhtemelen beyne sızan monosit türevi makrofajları bloke etmek, enflamatuar sitokin üretimini ve iltihaplanma aracılı doku hasarını nasıl azaltır?
KV1.3 Blokerlerin mikroglia işlevi üzerindeki etkileri
Kültürlenmiş neonatal fare ve sıçan mikrogliasının yanı sıra fare beyninden akut olarak izole edilmiş mikroglia veya sıçan beyninden doku baskılı mikroglia'nın, in vitro stimülasyonu veya in vivo stimülasyonu takiben önemli ölçüde artan tüm hücre patch-clamp ile KV1.3 akımlarını ifade ettiği gösterilmiştir. TLR-4 ligandı lipopolisakarit (LPS) ile intraserebroventriküler enjeksiyon [14–18]. Gram-negatif hücre duvarı bileşeni LPS ile stimülasyon, bakteriyel bir enfeksiyonla ilişkilendirilebilecek genel enflamasyonu simüle eden "klasik" aktive edilmiş "M1-benzeri" bir mikroglia durumunu indüklemek için yaygın olarak kullanılır [19,20]. Nöroimmünoloji alanında LPS ile uyarılan mikroglia, aşırı basitleştirilmiş olarak kabul edilen [21], ancak terapötik özelliği nedeniyle yaygın olarak kullanılan M1/M2 terminolojisini kullanmaktan kaçınmak için polarizasyonu indüklemek için kullanılan uyarana dayalı olarak ideal olarak M(LPS) mikroglia olarak adlandırılmalıdır. çekicilik
LPS ile stimülasyonun ardından artmış KV1.3 ekspresyonu, Western blotlama, immünohistokimya ve tüm hücre yama-kelepçesi ile ölçülen artan akım yoğunluğu ile mRNA seviyesinde ve protein seviyesinde gözlemlenebilir [15-18]. Kv1.3 ekspresyonunda benzer ancak biraz daha az yoğun bir artış, kültürlenmiş neonatal mikroglia, Alzheimer veya Parkinson hastalığında yanlış katlanan ve kümelenen iki protein olan oligomerik amiloid- (AO) veya -sinüklein [7,8] ile uyarıldığında ortaya çıkar ve genellikle ilgili hastalıkla ilişkili mikroglia tepkilerinin in vitro bir modelini oluşturmak için kullanılır.
Bu tip in vitro sistemlerde KV1.3 inhibisyonu veya genetik silinmesi, mikroglia aktivasyonunu takip eden 24- veya 48-saatlerde ölçülen birden çok enflamatuar aracının ifadesini ve üretimini azaltır. Yaklaşık 20 yıl önce Lyanne Schlichter'in laboratuvarı, KV1.3 inhibitörlerinin, kültürlenmiş neonatal sıçan mikrogliasında forbol esterle uyarılan solunum patlamasını [22] ve NO üretimini baskıladığını, böylece bir transwell kültür sisteminde mikroglia aracılı nöronal ölümü azalttığını bildirdi [16].

KV1.3 ve KCa3.1 blokerlerinin yaygın olarak kullanılan mikroglia inhibitörü minosiklin ile diferansiyel polarize neonatal fare mikrogliası üzerindeki etkilerini karşılaştıran laboratuvarımızdan daha yakın tarihli bir çalışmada [17], Kv1.3 inhibisyonunun ekspresyonu ve üretimi azalttığını gözlemledik. proinflamatuar sitokinler IL-1 ve TNF-'nin 24 ve 28. saatlerde ve enflamasyonla ilişkili enzimler siklooksijenaz2 (COX-2) ve indüklenebilir nitrik oksit sentazın (iNOS) yukarı regülasyonunu önledi. Sonuncu etki, muhtemelen LPS stimülasyonundan 24 ve 48 saat sonra KV1.3 inhibitörleri ile tedavi edilen mikrogliada gözlemlenen azalmış NO üretiminden sorumluydu. Önceki çalışmaya benzer şekilde, KV1.3 inhibitörlerinin, iskemik inmeyi simüle etmek için mikroglia 1-saatlik hipoksi/glisemi yoluyla etkinleştirildikten 3 gün sonra organotipik hipokampal dilim kültürlerinde mikroglia aracılı nöronal öldürmeyi önlediğini de gözlemledik [5] veya AD'de mikroglia aktivasyonunu simüle etmek için oligomerik amiloid- ile tedavi ederek [7].
CD11b veya Iba-1 için mikroglia boyanarak ve floresan yoğunluğunun değerlendirilmesiyle açıkça gösterilebilen bir olgu olan AO kaynaklı mikroglia aktivasyonunun azaltılmasına ek olarak, KV1.3 inhibitörü PAP-1'nin ayrıca önlediği bulunmuştur. Hipokampal dilimlerde O kaynaklı, mikroglia aracılı uzun vadeli güçlenme (LPT) bozukluğu ve kültürlenmiş fare mikrogliasında A O kaynaklı IL-1, TNF- ve NO üretimini azaltmak için [7], çok benzer LPS ile uyarılmış mikrogliaya sahip KV1.3 inhibitörleri için bulunanlara [17,18]. Yabani tip ve KV1.3-/- farelerinden kültürlenmiş neonatal fare mikrogliasının, her ikisi de farmakolojik KV1 olan model tanıma reseptörleri TLR2 ve CD36'ya [23] bağlanarak mikrogliayı aktive eden agregat -sinüklein (SynAgg) ile uyarıldığı deneylerde. 3 PAP-1 ile inhibisyon ve kanalın genetik olarak silinmesi, IL-1 , IL-6, IL-12 ve TNF- üretiminin azalmasına neden oldu ve 24'te NLRP3 enflamatuar protein yukarı regülasyonunu önledi mikroglia stimülasyonundan saatler sonra [8]. Tersine, bir mikroglial hücre hattında KV 1.3'ün aşırı ekspresyonu, stimülasyondan 24 saat sonra SynAgg kaynaklı IL-1, TNF-, IL-6 ve IL-12 ekspresyonunu veya salgılanmasını arttırdı [8].
Diğer gruplar tarafından yapılan çeşitli çalışmalar, KV1.3 blokerlerinin benzer uyaranlar veya diğer inflamatuar patolojilerle ilişkili uyaranlar kullanıldığında proinflamatuar mikroglia fonksiyonlarını azalttığını doğrulamıştır. Örneğin, HIV ile ilişkili nörobilişsel bozukluğu simüle etmek için HIV Tat proteini veya glikoprotein 120 (gp120) ile aktive edilen kültürlenmiş sıçan mikrogliasında, KV1.3 inhibisyonunun veya siRNA ile yok edilmesinin IL-1'yi azalttığı bulundu. , TNF- ve NO üretimi ve bastırılmış nörotoksisite [24,25]. Kültürlenmiş mikroglia'nın iskemik inme ve oksijen/glikoz yoksunluğu modelini kullanarak Ma ve ark. KV1.3 inhibisyonunun, mikroglial fenotipi proinflamatuar bir M1-benzeri yanıttan M2-benzeri bir yanıta kaydırdığını ve yukarıda açıklanan çalışmalara benzer şekilde NLRP3 inflamatuar aktivasyonunu azalttığını [5,6] bildirmiştir Parkinson hastalığı modellerinde [8].
KV1.3 bloke edici peptid ShK-223 varlığında ve yokluğunda sistemik olarak LPS ile tedavi edilmiş farelerin beyinlerinden hem CNS'ye sızan makrofajlardan hem de beyinde yerleşik mikrogliadan oluşan yeni izole edilmiş CD11b plus hücreleri kullanılarak, Rangaraju et al. KV 1.3 inhibisyonunun IL-1 gibi enflamatuar sitokinlerin ekspresyonunu azalttığını doğruladı, ancak KV1.3 inhibisyonunun ayrıca TAP1 ekspresyonunu azalttığını ve akış sitometrisi ile ölçüldüğü üzere CD11b artı CD45low mikrogliada EHD1'in yukarı regülasyonunu önlediğini gösterdi [26]. Hem TAP1 hem de EDH1, MHC sınıf-I montajında ve hücre yüzeyine kaçakçılığında yer alan proteinlerdir. Bu nedenle yazarlar daha sonra ShK-223 tedavisinin MHC sınıfı-1 ekspresyonu üzerindeki akut olarak izole edilmiş mikroglia üzerindeki etkisini araştırdılar ve azalan MHC ekspresyonuna dayanarak, mikrogliaların antijen sunma kapasitesinde LPS'nin neden olduğu artışlar olduğunu varsaydılar. mikroglia, KV 1.3-bağımlı süreçlerdir, bu da KV1.3 inhibisyonunun CD8 artı sitotoksik T hücrelerine antijen sunumunu azaltabileceğini düşündürmektedir.
Nöroinflamatuar ve nörodejeneratif hastalıklı fare modellerinden mikroglial transkriptomik veri kümelerine uygulanan sonraki bir ağırlıklı ortak ifade ağ analizinde, aynı grup KV1.3'ü Tlr2, Ptgs2, Il12b, Il1b, CD44, NFκB'yi de içeren bir proinflamatuar gen imzasının parçası olarak tanımladı. Stat1 ve RelA [27]. ShK-223 ile KV1.3 blokajı, bu proinflamatuar imzayı, hastalıkla ilişkili mikrogliada antiinflamatuar genlerin ekspresyonunun arttığı bir imzaya kaydırabilir. Bu bağlamda ilginç olan, diğer çalışmalarda anti-enflamatuar sitokinler IL-4 ve IL-10 ile uyarılan kültürlenmiş mikrogliaların göçünü daha da artırmak için Kv1.3 inhibitörlerinin rapor edilmiş olmasıdır [28] ve mikroboncukların mikroglial fagositozunu etkilememek [26] veya hatta amiloid- fagositozunu artırmak [7].

Birlikte ele alındığında, mikroglia'nın KV1.3'ü eksprese ettiğine ve KV1.3 blokerlerinin proinflamatuar, nörotoksik mikroglia fonksiyonlarını baskıladığına ve hatta mikroglia'yı daha nöroprotektif bir fenotipe doğru kaydırdığına dair yeterli kanıt vardır. Burada çoğunlukla kültürlenmiş mikroglial veya dilim kültürlerle elde edilen verileri özetlemeye odaklandık çünkü bu indirgemeci sistemlerde, nakavt, demonte veya farmakolojik blokajın etkisini doğrudan mikroglial KV1.3 kanallarının inhibisyonu yoluyla uyguladığına ve dolaylı olarak etkilemediğine dair hiçbir şüphe yoktur. Hepsi KV1.3'ü [29] eksprese eden T hücreleri, B hücreleri, dendritik hücreler veya monositlerdeki KV1.3 kanalları ve dolayısıyla KV1.3 blokerlerinin in vivo etkilerine veya KV1.3−/- ile yapılan bulgulara katkıda bulunabilir. fareler. Ancak burada belirtmek isteriz ki, kemirgenlerde ve insanlarda mikroglia üzerinde KV1.3 ifadesini immünohistokimya ile gösteren çok sayıda çalışmaya ek olarak, Kettenmann laboratuvarı ve grubumuz, aktifleştirilmiş mikroglia üzerinde artan KV1.3 ifadesinin sadece KV1.3 ifadesi olmadığını defalarca göstermiştir. bir doku kültürü fenomeni ve Kv1.3 akımlarının akut dilimlerdeki mikrogliadan [30,31] ve 5xFAD farelerinin beyinlerinden [7] veya orta serebral arter tıkanıklığından sonra enfarktüslü bölgeden [5, 12], iskemik inme için bir model.
KV1.3 inhibisyonundan veya Kv1.3 ekspresyonunu modüle etmekten etkilenen sinyal yolları
24 veya 48 saat sonra proinflamatuar mikroglia fonksiyonlarında bu faydalı azalmaları üretmek için KV1.3 blokerlerinden etkilenen sinyal yolaklarını (Şekil 1) araştıran çalışmalar, KV1.3 blokerlerinin etkilerinin bağımlı olduğunu düşündüren, biraz çelişkili sonuçlar vermiştir. uyarana ve belki de türe. Fordyce ve ark. KV1.3 blokerlerinin, LPS ile tedavi edilmiş neonatal sıçan mikrogliasında p38MAPK fosforilasyonunu etkilemediğini bildirmiştir [16], fare mikrogliasını kullanan diğer birkaç çalışma, KV1.3 blokerlerinin, stimülasyonu takiben NF-κB aktivasyonunun yanı sıra p38MAPK fosforilasyonunu ve aktivasyonunu güçlü bir şekilde azalttığını bulmuştur. LPS, AO, SynAgg veya HIV-1 glikoprotein 120 [7,8,24]. Mikroglial hücre hattında, BV2 KV1.3'ün ayrıca STAT1'in S727 fosforilasyonunu düzenlediği gösterilmiştir [26]. İlginç bir şekilde, KV1.3 blokerlerinin NFAT translokasyonunu inhibe edip etmediği, KV1.3 blokerlerinin T hücrelerinde en iyi incelenen etkilerinden biri [2,32,33] şimdiye kadar mikrogliada araştırılmamıştır.

Mikroglia'nın LPS, AO veya SynAgg ile uyarılmasının ardından KV1.3 ifadesindeki artışlar, KV1.3 inhibisyonundan etkilenen aynı sinyal kaskadlarının çoğunu içeriyor gibi görünmektedir ve KV1.3 blokerleri tipik olarak Kv1.3 ifadesindeki artışları önlemektedir. KV1.3 promotörü, birden fazla NF-κB ve SP1 bağlama bölgesi içerir ve NF-κB veya p38MAPK inhibitörleri, mikrogliada SynAgg tarafından uyarılan Kv1.3 yukarı regülasyonunu bağımsız olarak azaltır [8], hem p38MAPK hem de klasik NF-κB yollarının KV1.3'ün transkripsiyonel düzenlemesine aracılık eder (Şekil 1). Src ailesi kinaz Fyn, bileşeni p65'in [34] nükleer translokasyonunu düzenleyerek ve PKC izoformu PKCδ'yı fosforile ederek NF-κB transkripsiyon faktörünün yukarısında çalışır. Sarkar ve ark. Fyn nakavtının, kültürlenmiş mikrogliada KV1.3 akım yoğunluğunda hem LPS'yi hem de SynAgg'ın neden olduğu artışları azalttığını bildirdi; bu, mikroglia'nın Fyn inhibitörü saracatinib ile işlenmesiyle veya PKCδ eksikliğiyle taklit edilebilecek bir etki, Fyn/PKCδ kinaz sinyallemesinin kaskad, enflamatuar uyaranlara yanıt olarak KV1.3 yukarı regülasyonuna aracılık etmede rol oynar [8]. Bir Duolink yakınlık ligasyon tahlilinde gösterildiği gibi, Fyn doğrudan Kv1.3 ile etkileşime giriyor ve aktivitesini artırmak için Y135'te kanalı fosforile ediyor.
Kv1.3, zar potansiyelini düzenler ve depolarizasyona karşı direnç gösterir'
KV1.3 blokerlerinin in vivo nöroinflamasyon ve mikroglial sinyal kaskadları ve in vitro enflamatuar mediatör ekspresyonu ve sekresyonu üzerindeki yukarıda açıklanan iyi belgelenmiş iyileştirici etkilerine rağmen, KV1.3 blokerlerinin mikroglial fonksiyonları nasıl etkilediğine dair temel moleküler mekanizmalar uzun süredir belirsizdi. Laboratuvarımızın da dahil olduğu pek çok araştırmacı, KV1.3'ün mikrogliada T hücrelerinde yerine getirdiği işlevin aynısına hizmet ettiğini, yani membran potansiyelini ve kalsiyum akışını düzenlediğini varsaydılar [29,32,33].
T hücrelerinde KV1.3 inhibisyonu, membran depolarizasyonuna yol açar ve T hücresi reseptör stimülasyonunu takiben kalsiyum salınımıyla aktive olan kalsiyum kanalları (CRAC) yoluyla kalsiyum akışını azaltır [33,35,36]. CRAC kanalları yoluyla kalsiyum akışı, sitokin IL-2'nin [29,33] transkripsiyonunu tetikleyen kalsiyum/kalmodulin-bağımlı transkripsiyon faktörü NFAT'ın [29] fosforilasyonu ve müteakip nükleer translokasyonu için kritik olarak gereklidir. IL-2, sentez üzerine aktive edilmiş T hücrelerinden salınır ve otokrin ve parakrin tarzda T hücresi klonal genişlemesini uyarır. KV1.3 blokerleri, CRAC kanallarından kalsiyum akışını sürdürmek için gerekli olan dengeleyici potasyum akışını inhibe ederek, T hücrelerinin aktivasyonunu bozar, NFAT defosforilasyonunu ve nükleer translokasyonu [32] önler; [5,33,35,36].
Bununla birlikte, mikroglia'da hiç test edilmemişti, T hücrelerinden farklı olarak aynı zamanda içe doğru doğrultucu Kir2.1 [17,37,38] ve iki gözenekli potasyum kanalı THIK-1 (K2P 13.1) [39] ifade ediyor, KV1.3 blokerlerinin aynı moleküler etkilere sahip olup olmayacağı veya KV1.3'ün rolünün bu diğer potasyum kanalları tarafından üstlenilip üstlenilmediği. Yakın zamanda yapılan bir çalışmada, grubumuz buna göre önce KV1.3'ün dinlenme membran potansiyelini sürdürme ve depolarizasyona direnme konusundaki temel önemini yeniden inceleyerek bu soruyu ele aldı [40]. Beklendiği gibi, CHO hücrelerinde KV1.3'ün aşırı ekspresyonu, bu hücrelerin tipik olarak çok depolarize edilmiş dinlenme membran potansiyelini -20 mV'den -50 mV'ye düşürürken, ShK-223 depolarize mikroglia ile KV1.3 inhibisyonu, doğası gereği bir Elimizde ağırlıklı olarak Kir2.1'i eksprese eden farklılaşmamış mikrogliada ortalama -90 mV ve LPS'de -65 mV civarında olan daha hiperpolarize dinlenme membran potansiyeli, daha yüksek KV1.3 ve daha düşük Kir2.1 akım yoğunluklarını eksprese eden mikrogliayı uyardı [40].
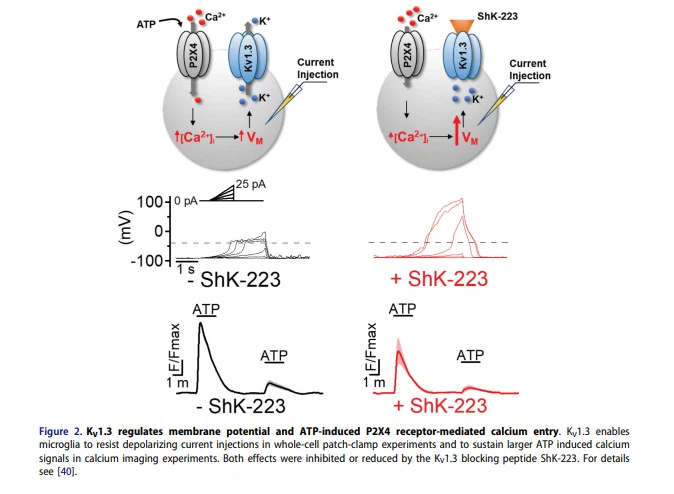
KV1.3 bu nedenle mikrogliada dinlenen zar potansiyelinin düzenlenmesine kesinlikle katkıda bulunurken (Şekil 2), daha önemli rolünün ve aktif mikrogliada Kv1.3 ifadesinin artmasının nedeninin, kanalın aşırı ve uzun süreli dengeleme yeteneği olduğuna inanıyoruz. mevcut enjeksiyon deneylerinin ortaya koyduğu gibi mikroglial sağlığı ve fizyolojiyi potansiyel olarak olumsuz etkileyebilecek membran depolarizasyonu. 25 pA'lık mevcut enjeksiyonlar, blokerlerin yokluğunda mikroglia ifade eden KV 1.3'ü -30 mV'nin ötesinde depolarize edemezken, KV 1.3 blokerlerle ön işleme tabi tutulan mikroglia, aynı 25 pA akım enjeksiyonlarına yanıt olarak artı 50 mV'lik potansiyellere depolarize olur [40] , KV1.3'ün aşırı membran depolarizasyonlarını önlemek için membran potansiyelini kanalın aktivasyon eşik potansiyeline yakın bir yere "kenetleyebileceğini" düşündürür (Şekil 2).
Mikroglial fizyolojide bu kapasitenin önemli olduğu durum, mikroglia'nın hücre dışı ATP'ye maruz kalmasıdır; bu, sitozolik ATP'nin hasarlı nöronlardan veya ATP içeren sinaptik veziküllerden salınması nedeniyle yüksek mikromolar aralıktaki konsantrasyonlara ulaşabilen bir tehlike sinyalidir [41], yoğun depolarizasyonlara yol açan P2X reseptör kanallarını aktive eden [42]. Kendi elimizde, farklılaşmamış ve LPS ile uyarılmış mikroglia üzerinde gerçekleştirilen mevcut kelepçe deneyleri, mikrogliada ifade edilen P2X reseptörlerinden birincil olarak P2X4'ü aktive eden 100 uM ATP'ye akut maruz kalmanın, farklılaşmamış mikrogliada daha belirgin depolarizasyonlara yol açtığını gösterdi. -40 mV'nin üzerinde depolarize olmayan KV1.3yüksek LPS ile uyarılmış mikrogliada olduğundan hiperpolarize dinlenme membran potansiyeli. KV1.3 blokerleri, ATP'nin indüklediği depolarizasyonlara ve onların varlığında depolarize olan mikroglialara karşı bu yeteneği bozmuştur [40].
KV1.3, mikrogliada P2X4 reseptör aracılı kalsiyum akışını modüle eder
Kalsiyum görüntüleme deneyleri, KV1.3 kanallarının ATP'nin neden olduğu P2X4- aracılı depolarizasyonlara direnme yeteneğinin, Ca2 artı 100 uM ATP ile uyarılan P2X4 reseptörleri aracılığıyla mikrogliaya girişi artırdığını ortaya çıkardı [40]. Örneğin, KV1.3 blokerleri ShK-223 ve PAP-1'in, yüksek KV1.3 akım yoğunluklarını ifade eden LPS ile farklılaştırılmış mikrogliada P2X4 reseptörleri yoluyla ATP'nin neden olduğu Ca2 artı akışını azalttığını gözlemledik, çok daha fazla LPS stimülasyonu, kültürlenmiş mikrogliada P2X4 reseptör ekspresyonunu aşağı doğru regüle etse de, uyarılmamış mikrogliadan daha güçlü. Buna karşılık, KV1.3 blokajının, çok düşük KV1.3 seviyeleri ifade eden IL-4 ile uyarılan mikrogliada ATP ile indüklenen geçici kalsiyum geçişleri üzerinde hiçbir etkisi olmamıştır. İlginç bir şekilde, LPS aynı zamanda in vivo mikroglia üzerinde KV1.3'ü arttırırken ve P2X4 ekspresyonunu azaltırken, hem KV1.3 hem de P2X4 ekspresyonu, laboratuvarımız tarafından farelerin enfarktüslü beyin yarımküresinden akut şekilde izole edilmiş mikroglia üzerinde gösterildiği gibi iskemik inme ortamında paralel olarak artar. immünohistokimya veya qPCR [5,12,43-46] ile kemirgen ve insan mikrogliasında iskemik inmeye ve diğer gruplara tabi tutulmuştur. Bu, aşağıdaki iskemik inme KV1.3'ün tehlike sinyali ATP tarafından başlatılan daha karmaşık pürinerjik mikroglial kalsiyum sinyalini in vitrodan daha güçlü bir şekilde düzenlediğini düşündürür. ATP ve beynin enfarktüs alanındaki diğer nöronal birikintiler mikroglia'yı aktive eder, bu mikroglia daha sonra 24 ila 72 saat içinde sürekli olarak daha fazla inflamatuar mediatör üretir ve serbest bırakır ve böylece penumbrada daha fazla nörona zarar verir ve öldürür ve enfarktüsün inflamatuar bir şekilde genişlemesine yol açar.
Enfarktüs sınırındaki mikrogliada 2-5 gün içinde gözlenen artmış KV1.3 ekspresyonu [5], muhtemelen aktive edilmiş mikroglianın artan sayıda P2X4 reseptörü aracılığıyla daha güçlü kalsiyum sinyallerini sürdürmesini ve böylece daha fazla enflamatuar aracı üreterek daha fazla nörona zarar vermesini sağlar. ve daha fazla mikrogliayı aktive etmek. Bu hipotez, KV1.3 bloker PAP-1'nin mikroglia aktivasyonunu ve beyin IL-1 ve IFN- seviyelerini düşürdüğü, kabaca yüzde 40 daha küçük enfarktüs alanlarına ve gelişmiş nörolojik hasara yol açtığı bulgusu ile uyumlu olacaktır. hem fare hem de sıçan iskemik inme modellerinde skorlar [5]. Kv1.3 blokerleri, mikrogliayı depolarize ederek, hasarlı nöronlardan salınan ATP tarafından tetiklenen P2X4 reseptörleri yoluyla kalsiyum akışını azaltır ve böylece NLRP3 inflamatuar, NF-κB ve diğer transkripsiyon faktörlerinin daha fazla kalsiyuma bağlı aktivasyonunu azaltarak inflamatuar aracı üretiminin azalmasına yol açar (Şekil 1) ve azaltılmış patoloji.
Mikrogliada başka hangi kalsiyum akış yolları KV1.3 tarafından düzenlenir?
KV1.3 blokajı, P2X4 reseptörleri yoluyla [40] ATP'nin neden olduğu kalsiyum akışını açık bir şekilde azaltmış ve bu nedenle mikrogliadaki bu kalsiyum akış yolunun önemli bir düzenleyicisini oluşturmuş olsa da (Şekil 2), bu, KV1.3 veya ATP'ye bağlı tek kalsiyum sinyali değildir. Mikrogliada süreç. P2X reseptör kanallarına ek olarak mikroglia, ATP veya UTP tarafından aktivasyonun ardından dahili depolardan kalsiyum salınımını indükleyebilen [47] ve nispeten küçük hücre içi kalsiyum depolarının tükenmesini takiben mağaza tarafından işletilen Ca2 artı girişini (SOCE) etkinleştirebilen metabotropik P2Y pürinerjik reseptörlerini de ifade eder. mikrogliada [38]. Bu nedenle, ek SOCE'nin, görüntülediğimiz ATP kaynaklı Ca2 plus sinyallerine katkıda bulunması ve KV1.3 bloke edici etkilerin bazılarına ek olarak SOCE'yi azaltarak aracılık etmesi kesinlikle mümkündür.
Bu çok muhtemel bir hipotezdir, çünkü T hücrelerinde KV1.3 blokerleri için "klasik" moleküler mekanizma, T hücresi reseptörü aktivasyonunu takiben CRAC kanalları aracılığıyla SOCE'nin azalması ve ardından transkripsiyon faktörü aktivasyonunun ve sitokin üretiminin ve salınımının azalmasıdır [29,33, 36,48]. Sıçan ve fare mikrogliasının, CRAC akımları için tipik biyofiziksel özelliklere sahip akımlar sergilediği [49,50] ve CRAC kanalları, Orai ve STIM'in [51,52] moleküler bileşenlerini ifade ettiği defalarca bildirilmiştir. Ayrıca Orai1, STIM1 ve STIM2'nin genetik olarak silinmesinin CRAC akımını ve/veya SOCE'yi azalttığına ve kültürlenmiş fare mikrogliasında göçü ve fagositozu inhibe ettiğine dair kanıtlar vardır [52], öte yandan küçük molekül CRAC kanal blokeri CM-EX-137 son zamanlarda bir fare travmatik beyin hasarı modelinde mikroglia aktivasyonunu ve lezyon boyutunu azalttığı bildirilmiştir [53].
KV1.3 kanallarının blokajı, LPS ile uyarılan mikrogliada depo tarafından işletilen kalsiyum girişini azaltır
KV1.3'ün P2X4 aracılı kalsiyum akışını düzenlemedeki rolüne ilişkin önceki makalemizin devamı niteliğinde bir deney olarak, burada özellikle KV1.3 bloke edici ShK-223'nin LPS farklılaştırılmış mikrogliada SOCE'yi azaltıp azaltmayacağı sorusunu sorduk. , en yüksek KV1.3 akım yoğunluklarını ve KV1.3 inhibisyonunun ATP ile indüklenen kalsiyum sinyali üzerindeki en büyük etkilerini gözlemlediğimiz aynı stimülasyon koşulu [40]. Serbest hücre içi kalsiyum konsantrasyonundaki ([Ca2 plus ]i) değişiklikleri izlemek için oranmetrik kalsiyum göstergesi Fura-2'yı kullanarak, LPS ile farklılaşmış mikroglia'nın 60 nM ve 370 nM, ortalama 150 ± 8,8 nM (n=50; Şekil 3a,c,g), bu önceki bir raporla tutarlıdır [54]. SOCE'yi ortaya çıkarmak için, hücre içi kalsiyum depoları önce, nominal olarak Ca2 artı içermeyen bir banyo solüsyonunda uygulanan, endoplazmik retikulum Ca2 artı -ATPaz'ın bir blokeri olan thapsigargin (Tg) ile tüketildi.
Removal of extracellular calcium produced a roughly 25 nM decrease in [Ca2+] I (Figure 3a) indicating the presence of a calcium influx at rest. Subsequent application of Tg (1 μM) elicited small amplitude (>25 nM) depolardan pasif kalsiyum mobilizasyonuna bağlı olarak [Ca2 plus ] I'de eşzamansız yükselmeler. Kalsiyumun banyo solüsyonuna yeniden eklenmesi, [Ca2 plus ]I'de SOCE'nin neden olduğu dinlenme seviyelerinin üzerinde hızlı bir yükselmeye neden oldu. CA2 artı içermeyen banyo solüsyonundaki [Ca2 artı ] I seviyesi ile kalsiyumun yeniden eklenmesini takiben maksimal [Ca2 artı ] I yükselmesi arasındaki fark olarak ölçülen SOCE kaynaklı [Ca2 artı ] I geçişlerinin ("en yüksek SOCE") büyüklüğü değişti 120 nM'de maksimum ve 1800 nM'ye kadar bir kuyruk gösteren tepe SOCE dağılımına sahip bireysel hücreler arasında önemli ölçüde (Şekil 1b). SOCE'nin gücündeki bu heterojenliğe, muhtemelen SOCE sırasında kalsiyum girişi için itici güç sağlayan dinlenme membran potansiyelindeki değişiklikler neden olur. LPS ile farklılaştırılmış mikroglia'nın dinlenme membran potansiyelinin, tek tek hücrelerde -90 mV ile -40 mV arasında değiştiği bulunmuştur [40,55] ve bu nedenle, SOCE'de gözlemlenen farklılıkları açıklayabilir.

Daha önceki bir çalışma, istirahat [Ca2 artı ]I'deki yükselmenin, P2Y reseptörü agonisti UTP veya tamamlayıcı faktör 5a gibi LPS ile aktive olan mikrogliada [Ca2 artı ]I geçişlerini ortaya çıkarmak için azalan dış uyaranlarla ilişkili olduğunu bildirmiştir [54]. Çalışmamızda hem istirahat [Ca2 artı ]i seviyeleri hem de pik SOCE değerleri tek tek hücreler arasında farklılık gösterdiğinden, istirahat [Ca2 artı ]i'deki varyasyonun pik SOCE değerlerindeki heterojenliği açıklayıp açıklamadığını araştırdık. İstirahat [Ca2 artı ] I'e karşı pik SOCE değerlerinin çizilmesi, pik SOCE ile dinlenme [Ca2 artı ] I arasında pozitif bir korelasyon ortaya çıkardı (Şekil 3c). Verileri zirve SOCE için 600 nM kesme değeriyle iki gruba ayırdığımızda, her gruptaki dinlenme [Ca2 artı ]I ve zirve SOCE arasındaki ilişkiler tüm popülasyondakinden daha güçlüydü, bu da en az iki hücrenin varlığını gösteriyor. hem SOCE'nin büyüklüğü hem de dinlenme [Ca2 plus ] I ile tepe SOCE arasındaki korelasyonun gücü bakımından farklılık gösteren popülasyonlar. Bu nedenle, LPS ile tedavi edilen hücrelerin popülasyonunda, dinlenme [Ca2 artı]i'deki bir artış, daha önce öne sürüldüğü gibi, aktifleştirilmiş mikroglia'nın dış uyaranlara geçici bir [Ca2 artı]I ile yanıt verme yeteneğinin azalmasıyla nedensel olarak bağlantılı değildir. Hoffman ve ark. Verilerimiz, KV1.3, Kir2.1 ve THIK-1 dahil olmak üzere çeşitli kanallar tarafından kontrol edilen membran potansiyeli seviyesi gibi ortak bir etkinin, arasındaki pozitif korelasyondan sorumlu olabileceğini düşündürmektedir. dinlenme [Ca2 plus ] I ve pik SOCE çalışmamızda gözlendi. Örneğin, hiperpolarize edici kanalların aşırı ekspresyonu veya fonksiyonel yukarı regülasyonu, zarı hiperpolarize edebilir ve hem metabolik olarak aktifleştirilmiş geçici reseptör potansiyeli (TRP) kanalları hem de mağazanın tükenmesini takiben aktive edilen mağaza tarafından işletilen kanallar gibi yapısal olarak aktif kalsiyum geçirgen kanallar yoluyla kalsiyum girişi için itici gücü artırabilir. CRAC kanalları gibi.
Pre-incubation of cells with the KV1.3 inhibitor ShK-223 did not significantly affect resting [Ca2+] I (Figure 3d,g), but eliminated peak SOCE responses larger than 300 nM and shifted the maximum of the distribution of peak SOCE values from 130 nM (Figure 3b, control) to 70 nM (Figure 3e, ShK223). The difference between the values of peak SOCE in control cells and cells preincubated with ShK-223 was significant (Figure 3h). The relationship between resting [Ca2+] I and peak SOCE still displayed a mild positive correlation (figure 3f). Taken together, our data indicate that similarly to T lymphocytes, blockade of KV1.3 channels significantly reduces SOCE in LPS differentiated microglia. The extent of the inhibition varied among cells with a greater effect on cells expressing large magnitude (>300 nM) SOCE. Yüksek ve düşük zirve SOCE'ye sahip hücrelerin spesifik özellikleri henüz belirlenmemiştir.
Fizyolojik koşullar altında SOCE, G-protein eşli P2Y reseptörlerinin aktivasyonunu takiben tükenmeyi depolamak için daha sonra tetiklenebilir ve ATP gibi yaygın pürinerjik agonistler tarafından ortaya çıkarılan P2Y ve P2X reseptörlerinin aktivasyonu sırasında kombine [Ca2 artı] I yükselmesine katkıda bulunur. SOCE'nin büyüklüğü, depo tarafından çalıştırılan kanalların ve KV1.3 gibi membran potansiyelini kontrol eden kanalların diferansiyel ekspresyonunun benzersiz kombinasyonunun bir fonksiyonu olabilen LPS farklılaştırılmış hücreler arasında önemli ölçüde değişiklik gösterir. Zirve SOCE'de ShK-223 ile azalma, KV1.3 kanallarının güçlü SOCE düzenleyicileri olduğunu gösterir ve KV1.3 blokerlerinin kalsiyum sinyalini ve kalsiyuma bağlı transkripsiyonu takiben sonraki fonksiyonel tepkileri (örn. sitokin üretimi) zayıflattığı ek bir mekanizmayı ortaya çıkarır. mikrogliada faktör aktivasyonu.

Sonuçlar
KV1.3 blokerlerinin CNS'deki inflamasyon üzerindeki yararlı etkilerini yapmak için özellikle hafıza T hücreleri ve monosit türevli makrofajlar üzerindeki katkının periferik bağışıklık sistemi hücreleri üzerindeki etkilerini sıralamak kesinlikle zor olsa da, KV1.3'ün membran potansiyelini düzenlemede, depolarizasyonu önlemede ve daha sonra mikroglia aktivasyonuna ve enflamatuar mediatör üretimine yol açan kalsiyum sinyal olaylarını kontrol etmede önemli roller oynadığı açıktır. Terapötik bir bakış açısıyla, KV1.3'ün çoklu bağışıklık sistemi hücre tiplerinde inhibe edilmesinin muhtemelen arzu edilir olduğunu önermek isteriz. Bununla birlikte, KV1.3 inhibitörlerinin ana hücresel hedefinin ne olduğunu ve terapötiklerin CNS hastalıklarında optimal iyileştirici etkiler sergilemek için beyne nüfuz etmesi gerekip gerekmediğini açıklığa kavuşturmak, terapi gelişimi için entelektüel olarak çok tatmin edici ve yararlı olacaktır. Bu sorular, ideal olarak, Alzheimer ve Parkinson hastalığının hayvan modellerinde periferik olarak kısıtlanmış peptidik KV1.3 inhibitörleri veya anti-KV1.3 antikorları [58,59] ile beyne nüfuz eden küçük molekülleri yan yana test ederek farmakolojik olarak ele alınmalıdır. Nöroinflamasyonda KV1.3'ün rolünü daha ayrıntılı bir şekilde anlamak için mikroglia, monosit türevi makrofajlar ve farklı T hücre alt kümelerindeki koşullu KV1.3 silinmesinin etkilerini ilaç tedavisinin etkileriyle karşılaştırmak ayrıca oldukça bilgilendirici olacaktır. ve KV1.3 inhibitörlerinin hücresel hedefi. Bununla birlikte, hücresel düzeyde, KV1.3'ün temel rolünün her zaman ilk olarak T hücrelerinde açıklanan şey, yani membran potansiyeli ve kalsiyum akışının düzenlenmesi ve ardından kalsiyuma bağımlı transkripsiyon faktörlerinin aktivasyonu olacağına inanıyoruz. Bu açıdan bazen yeterince vurgulanmayan şey, muhtemelen KV1.3'ün yarı aktivasyon voltajı ve nispeten yavaş inaktivasyonu [60,61] gibi biyofiziksel özelliklerinin, kanalı membran depolarizasyonlarına direnmek ve dolayısıyla KV1'i etkinleştirmek için mükemmel şekilde "niteliklendirmesi"dir. .3, 30 yıl önce T hücrelerinde tarif edildiği gibi sadece SOCE'yi değil, aynı zamanda P2X reseptör aracılı kalsiyum akışını da düzenler.
Açıklama bildirimi
Yazarlar tarafından herhangi bir potansiyel çıkar çatışması bildirilmemiştir.
Finansman
Bu çalışma, Ulusal Nörolojik Hastalıklar ve İnme Enstitüsü ödülü NS100294 (HW'ye) ve UC Davis Tıp Fakültesi Araştırma Ortaklığı Hibesi (AFF'ye) tarafından desteklenmiştir.
Referanslar
[1] DeCoursey TE, Chandy KG, Gupta S, et al. İnsan T lenfositlerinde voltaj kapılı K artı kanalları: mitogenezde bir rolü var mı? Doğa. 1984;307(5950):465–468.
[2] Beeton C, Wulff H, Standifer NE, et al. Kv1.3 kanalları, T hücresi aracılı otoimmün hastalıklar için terapötik bir hedeftir. Proc Natl Acad Sci USA. 2006;103 (46):17414–17419.
[3] Tarcha EJ, Chi V, Munoz-Elias EJ, et al. Otoimmün hastalığın T hücre aracılarını baskılayan spesifik bir Kv1.3 kanal inhibitörü olan ShK-186 peptitinden gelen dayanıklı farmakolojik tepkiler. J Pharmacol Uzm. 2012;342(3):642–653.
[4] Chandy KG, Norton RS. Otoimmün hastalık için terapötik olarak T hücrelerinde Kv1.3 kanallarının peptid blokerleri. Curr Opin Chem Biol. 2017;38:97–107.
[5] Chen YJ, Nguyen HM, Maezawa I, et al. Potasyum kanalı Kv1.3'ün inhibisyonu, iskemik inmede enfarktüsü ve enflamasyonu azaltır. Ann Clin Transl Neurol. 2018;5(2):147–161.
[6] Ma DC, Zhang NN, Zhang YN, ve ark. Kv1.3 kanal blokajı, M1/M2 fenotiplerini yeniden şekillendirerek ve mikrogliada NLRP3 inflamatuar aktivasyonunu tehlikeye atarak serebral iskemi/reperfüzyon hasarını hafifletir. Uzman Neurol. 2020;332:113399.
[7] Maezawa I, Nguyen HM, Di Lucente J, et al. Alzheimer hastalığı için potansiyel bir mikroglia hedefli tedavi olarak Kv1.3 inhibisyonu: klinik öncesi kavram kanıtı. Beyin. 2018;141(2):596–612.
[8] Sarkar S, Nguyen HM, Malovic E, et al. Kv1.3, Parkinson hastalığında nöroinflamasyonu ve nörodejenerasyonu modüle eder. J Clin Invest. 2020;130 (8):4195–4212.
[9] Reeves TM, Düzeltici PA, Colley BS, et al. Travmatik beyin hasarından sonra beyaz cevher patolojisini azaltmak için Kv1.3 kanallarını hedefleme. Uzman Neurol. 2016;283(PtA):188–203.
[10] Lai IK, Valdearcos M, Morioka K ve ark. Kv1.3 potasyum kanallarının bloke edilmesi, farelerde yara iyileşmesini bozmadan postoperatif nöroinflamasyonu ve bilişsel gerilemeyi önler. Br J Anaesth. 2020;125 (3):298–307.
[11] Peng Y, Lu K, Li Z ve ark. Kv1.3 kanallarının blokajı, radyasyona bağlı beyin hasarını iyileştirir. Nöro Onkol. 2014;16(4):528–539.
[12] Chen YJ, Nguyen HM, Maezawa I, et al. Potasyum kanalı KCa3.1, iskemi/reperfüzyon inme ile ilişkili nöroinflamasyon için farmakolojik bir hedef oluşturur. J Cereb Kan Akışı Metab. 2016;36 (12):2146–2161.
[13] Rangaraju S, Gearing M, Jin LW, et al. Potasyum kanalı Kv1.3, insan Alzheimer hastalığında mikroglia tarafından yüksek oranda ifade edilir. J Alzheimer Dis. 2015;44 (3):797–808.
[14] Norenberg W, Gebicke-Haerter PJ, Illes P. Enflamatuar uyaranlar, kültürlenmiş sıçan mikrogliasında yeni bir K artı dışa doğru akımı indükler. Neurosci Lett. 1992;147 (2):171–174.
[15] Kotecha SA, Schlichter LC. Endojen hipokampal mikrogliada Kv1.5'ten Kv1.3'e geçiş ve proliferasyonda rol. J Nörobilim. 1999;19(24):10680–10693. [16] Fordyce CB, Jagasia R, Zhu X, et al. Microglia Kv1.3 kanalları, nöronları öldürme yeteneklerine katkıda bulunur. J Nörobilim. 2005;25(31):7139–7149.
[17] Nguyen HM, Grossinger EM, Horiuchi M, et al. "Klasik" ve "alternatif olarak" aktive edilmiş mikrogliada diferansiyel Kv1.3, KCa3.1 ve Kir2.1 ifadesi. glia. 2017;65(1):106–121.
For more information:1950477648nn@gmail.com
